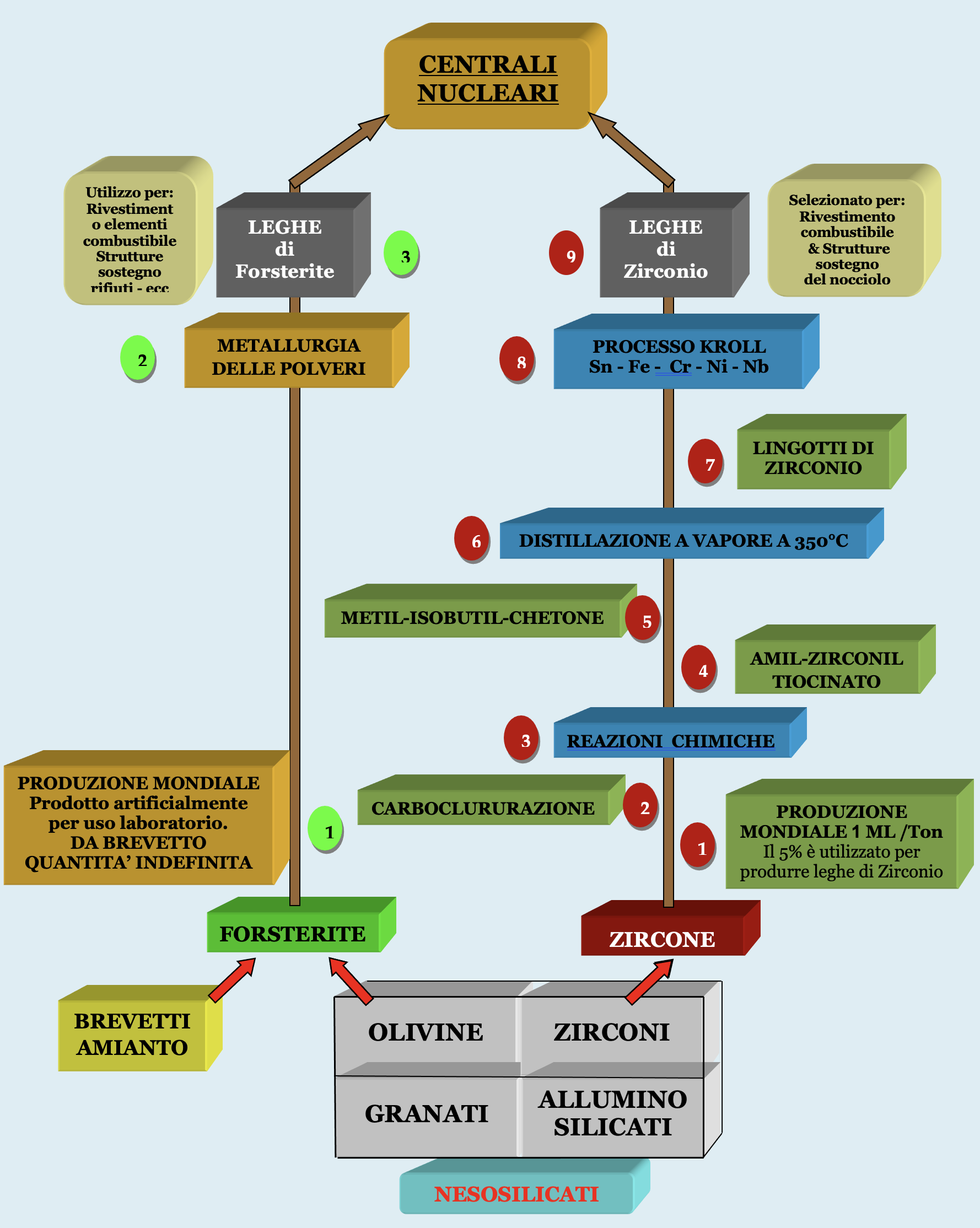
...A confronto
Forsterite verso Zirconio
Le ridotte capacità di approvvigionamento e gli elevati costi energetici di produzione dello Zirconio ci hanno spinto a “designare” la Forsterite elemento indispensabile nelle varie applicazioni dell’industria nucleare e per lo smaltimento delle scorie radioattive.
La Forsterite, il prezioso elemento generato dal trattamento di inertizzazione dell’Amianto, attraverso il forno ad atmosfera controllata.

NESOSILICATI A CONFRONTO
(minerali con struttura cristallina isolata)
FORSTERITE (Mg2.SiO4) Silicato di Magnesio
ZIRCONE (Zr.SiO4) Silicato di Zirconio
FORSTERITE
Produzione annua: dato non disponibile – Minerale Raro
Prezzo: fino a €.100 al carato (o,2gr.)
Punto di Fusione: 1890°c
Si trova nelle rocce magmatiche povere di silice (ignee mafiche ed ultramafiche); é anche presente in rocce metamorfiche di tipo dolomitico e in alcune meteoriti.
Configurazione: Metallo Alcalino Terroso
Dov’è utilizzato: come Biomateriale (test sostituzione protesi Titanio) – in Biotecnologie (test collanti alte temperature) – Pietre e Gioielli (gemme) – materiali Dielettrici (test apparati ad alta frequenza -pellicole).
Impieghi del Magnesio Metallico:
E’ il terzo metallo più utilizzato nelle costruzioni dopo Ferro e Alluminio; quasi il 70% della produzione mondiale di Magnesio viene utilizzata per produrre leghe che hanno una densità molto bassa, una resistenza elevata e un’eccellente lavorabilità; usi principali in aereonautica, componenti per auto, industria dell’Alluminio, Anodi Sacrificali (protezione degli scafi navali e sottomarini, piattaforme petrolifere e condutture dalla corrosione; il 10% della produzione mondiale è utilizzato per la produzione del Titanio; I composti di Magnesio sono utilizzati come materiale refrattario in fornaci per la produzione di Ferro e Acciaio, dei Metalli non Ferrosi, di Vetro e Cemento;
Impieghi del Calcio Metallico:
Viene utilizzato in lega con il litio, negli acciai e nelle leghe di Rame e Nichel; come desolforante e decarburante in vari acciai e leghe speciali; per eliminare tracce di Azoto e Ossigeno dai Gas Nobili; per ottenere metalli pregiati tramite riduzione dei loro Ossidi; per la preparazione dell’Idruro; in Acciai e leghe di Alluminio, Zinco, Magnesio e Piombo.
Privative Industriali Tuccitto
UIBM n°30653/20
EPO n°EP21425060.7
Crisotilo > Metacrisotilo > Forsterite
Inertizzazione > Metallurgia delle Polveri > Sinterizzazione = produzione di Metalli di Magnesio e di Calcio (dal trattamento di Cemento Amianto = Larnite Nesosilicato di Calcio + Forsterite) e fabbricazione di Leghe speciali con uso di ossidi metallici, carbonio etc.
Applicazioni Leghe di Forsteritio:
Industria Aerospaziale – Impianti & Centrali Nucleari – Smaltimento Scorie – Industria Bellica – Pneumatici Tessuti Speciali – Composti Plastici – Automotive – Materiali Ignifughi – Industria del Legno – Elettronica – Ingegneria Civile – Edilizia & Infrastrutture – Industria Navale – Preziosi & Gioielli – Bio e Nanotecnologie, etc.
ZIRCONE
Produzione annua: circa 1.ml.ton.
Prezzo: da €.15 a €.40 al carato (0,2 gr.)
Punto di Fusione: 1855°c
Si rinviene nelle rocce vulcaniche basiche o femiche (pegmatiti e rocce filoniane alcaline); si trova anche nelle rocce metamorfiche.
Configurazione: Metallo di Transizione
Usi Conosciuti: nei Preziosi (gemme in oreficeria) – Biomateriali (protesi dentarie) Produzione di Leghe di Zirconio (per il rivestimento delle barre di combustibile e barre di sostegno nelle Centrali Nucleari)
Fasi per la produzione di Zirconio:
1) lo Zircone viene bollito in una soluzione di Idrossido di Sodio (digestione alcalina) per formare Zirconia o Biossido di Zirconio.
2) Il Biossido viene fatto reagire con Coke in un arco elettrico per formare Carbonitruro di Zirconio e quindi con Cloro per formare Tetracloruro di Zirconio
3) Il Tetracloruro di Zirconio viene ridotto in metallo di Zirconio nel Processo Kroll con Magnesio in atmosfera di Elio.
La polvere di Zirconio è infiammabile, il lingotto no. Il valore della polvere può raggiungere le 200.000 €. / ton.
In alternativa il processo Van.Arkel-de-Boer che si basa sulla formazione reversibile di Ioduri che si ricompongono in Metallo puro: Il Titanio viene fatto riscaldare in un crogiuolo fino a 800°c in presenza di Iodio fondendo e formando Ioduro di Titanio. Questi a pressione atmosferica si volatilizzava formando Tetraioduro di metallo gassoso che viene posto a contatto con filamenti di Tugsteno e riscaldato ad arco fino a 1400°c da cui si deposita metallo fuso. Il processo può durare da diverse ore a settimane. Lo Zirconio si ottiene anche come sottoprodotto della lavorazione dei minerali di Titanio ovvero dal Magnesio Metallico.
Applicazioni Lega di Zirconio:
Lo Zirconio viene soprattutto aggiunto in alcune leghe per renderle più resistenti. Esempio, vista la resistenza alle alte temperature e alla corrosione, è utilizzato come rivestimento per barre di combustibili nucleari contenenti Uranio 235, Uranio 238 e Plutonio nelle varie concentrazioni.
Lo Zirconio: applicazioni e pericolosità
Quanto segue per considerare, viste le caratteristiche pressoché coincidenti tra Forsterite e Zircone, che gli utilizzi di quest’ultimo potrebbero essere ulteriormente sviluppati anche per le qualità del Magnesio, rappresentato dalla Forsterite contro un appartenente allo stesso Gruppo di Nesosilicati, lo Zircone, che spesso in natura risulta essere un elemento radioattivo per la sua vicarianza all’Uranio.
Lo Zirconio è un metallo di transizione che si colloca al 4° gruppo della Tavola Periodica, sotto il Titanio e sopra l’Afnio; non si trova libero in natura allo stato metallico ma si trova contenuto in un minerale, lo Zircone, da cui prende il nome.
A causa delle impurità dell’Afnio contenute nello Zirconio, se ne rende necessaria una separazione quasi completa estraendolo dallo Zirconio. Le proprietà fisiche e chimiche dei due elementi sono molto simili. Sono stati sviluppati processi di estrazione liquido-liquido con un’ampia varietà di solventi che sono ancora utilizzati per la produzione dell’Afnio. Circa la metà di tutto l’Afnio metallico prodotto è ottenuto come sottoprodotto della raffinazione dello Zirconio. Il prodotto finale della separazione è il Cloruro di Afnio. Il Cloruro di Afnio purificato viene convertito nel metallo, per riduzione, con Magnesio o Sodio, come nel processo Kroll per la produzione di metalli di Zirconio.
L’Afnio viene poi utilizzato in leghe con Ferro, Titanio, Niobio, Tantalio e altri metalli per usi altamente ricercati come per gli ugelli del propulsore a razzo a propellente liquido, ad esempio nel motore principale dei moduli lunari. Fra le tante, la lega C103 formata dall’89% di Niobio, dal 10% di Afnio e dall’1% di Titanio.
Lo Zirconio metallico in polvere è altamente infiammabile, tuttavia la forma solida è molto meno soggetta all’accensione. Lo Zirconio è resistente alla corrosione di acidi, alcali, acqua salata e altri agenti. Si scioglie in Acido Cloridrico e Solforico, specialmente in presenza di Fluoro. Il punto di fusione è 1855 °C.
Lo Zirconio si ottiene anche come sottoprodotto dell’estrazione e della lavorazione dei minerali di Titanio Ilmenite (Titanato di Ferro FeTiO3) e Rutilo (Biossido di Titanio TiO2), oltre che direttamente dallo Zircone attraverso vari processi chimici
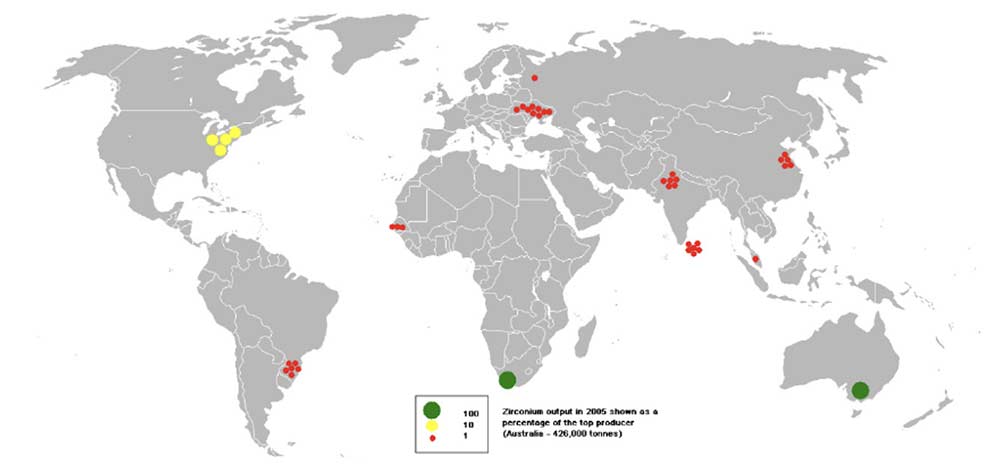
Lo Zircone si trova abbondante in Australia, Brasile, India, Russia, Sudafrica, Stati Uniti e Ucraina. Nonostante le risorse mondiali superino i 60 milioni di tonnellate in tutto e la produzione annuale mondiale di Zirconio, nel 2013 è stata di circa 1,5 milioni di tonnellate.
Principali depositi di Zirconio nel Mondo (2005)
Applicazioni dello Zirconio
La maggior parte degli Zirconi viene utilizzata direttamente come materiale resistente ad alta temperatura. Infatti lo Zircone è refrattario, duro e resistente agli attacchi chimici. Un suo uso principale è come opacizzante, poiché fornisce un aspetto bianco e opaco ai materiali ceramici. Poiché possiede un’alta resistenza chimica, lo Zircone è utilizzato anche in ambienti aggressivi, come gli stampi per metalli fusi.
Il Biossido di Zirconio (ZrO2) o zirconia è utilizzato nei crogioli di laboratorio, nei forni metallurgici e come materiale refrattario. Poiché è meccanicamente resistente e flessibile, può essere sinterizzato in coltelli o altre lame in ceramica. La Zirconia è un componente di alcuni abrasivi usati nella carta vetrata e nelle mole.
La Zirconia Cubica o Zircone Bianco (ZrSiO4) viene lavorata e tagliata in pietre preziose per l’uso in gioielleria, come sostituto del Diamante.
Una frazione dello Zircone minerale estratto è convertita in metallo, che trova varie applicazioni di nicchia. Per la sua eccellente resistenza alla corrosione è spesso utilizzato come agente legante in materiali esposti ad ambienti aggressivi, come apparecchi chirurgici, filamenti leggeri e casse per orologi.
L’elevata reattività dello Zirconio con l’Ossigeno ad alte temperature viene impiegata in alcune applicazioni specializzate come innesco di esplosivi e assorbente in tubi a vuoto. La stessa proprietà è sfruttata includendo nanoparticelle di Zr come materiale piroforico in armi esplosive, come la BLU-97 / B Combined Effects Bomb.
Il Biossido di Zirconio, composto con il Tungsteno, Tungstato di Zirconio, ha l’insolita proprietà di restringersi quando riscaldato, mentre la maggior parte delle altre sostanze si espande con il calore.
I composti con Carbonio e Azoto, rispettivamente Carburo di Zirconio e Nitruro di Zirconio, sono solidi usati come refrattari.
Il composto di Titanio, Zirconio e Piombo, indicato con la sigla PZT, è il materiale piezoelettrico più comunemente usato, con applicazioni quali trasduttori ultrasonici, idrofoni, iniettori, e trasformatori piezoelettrici.
Lo Zirconio è anche un componente di alcuni catalizzatori Ziegler–Natta, usati per produrre Polipropilene. Questa applicazione sfrutta la capacità dello Zirconio di formare in modo reversibile legami con il Carbonio.
Applicazioni nelle Centrali Nucleari
Il rivestimento dei carburanti per reattori nucleari consuma circa l’1% dell’approvvigionamento di zirconio o sue leghe o sotto forma di zirconi. Le proprietà desiderate di queste leghe sono una bassa sezione di cattura dei neutroni e resistenza alla corrosione in normali condizioni di servizio.
Uno svantaggio delle leghe di zirconio è che questo reagisce con l’acqua ad alte temperature, producendo idrogeno gassoso e degradazione accelerata del rivestimento delle barre di combustibile:
Zr + 2H2O → ZrO2 + 2 H2
Questa reazione esotermica è molto lenta al di sotto di 100 °C, ma a temperature superiori a 900 °C avviene rapidamente. La maggior parte dei metalli subisce reazioni simili. Questa reazione fu responsabile di una piccola esplosione di idrogeno osservata per
la prima volta all’interno dell’edificio del reattore della centrale nucleare di Three Mile Island nel 1979, ma a quel tempo l’edificio di contenimento non fu danneggiato. La stessa reazione si è verificata nei reattori 1, 2 e 3 della centrale nucleare di Fukushima I (Giappone) dopo che il raffreddamento del reattore fu interrotto dal disastro del terremoto e dello tsunami dell’11 marzo 2011, con conseguente incidente nucleare. Dopo aver scaricato l’idrogeno nella sala di manutenzione di quei tre reattori, la miscela di idrogeno con ossigeno atmosferico esplose, danneggiando gravemente gli impianti e almeno uno degli edifici di contenimento. Per evitare l’esplosione, la ventilazione diretta dell’idrogeno nell’atmosfera aperta sarebbe stata un’opzione di progettazione preferita.
Ora, per prevenire il rischio di esplosione in molti edifici di contenimento del reattore ad acqua pressurizzata (PWR), è installato un ricombinatore che converte Idrogeno e Ossigeno in acqua a temperatura ambiente prima che si verifichi il pericolo.
I materiali fabbricati in Zirconio Metallico sono utilizzati nei veicoli spaziali che richiedono resistenza al calore.
Parti che devono sopportare temperature elevate come combustori, pale e palette nei motori a reazione e nelle turbine a gas fisse vengono sempre più spesso protette da sottili strati di ceramica, generalmente rivestiti da uno strato di zirconia e ittria, ossido di ittrio.
Applicazioni biomediche
I composti contenenti Zirconio sono utilizzati in molte applicazioni biomediche, tra cui impianti e corone dentali, protesi di ginocchio e anca, ricostruzione della catena ossicolare dell’orecchio medio e altri dispositivi protesici.
Lo Zirconio si lega all’urea, una proprietà che è stata ampiamente utilizzata a beneficio dei pazienti con malattia renale cronica. Ad esempio, lo Zirconio è un componente primario della colonna assorbente nel sistema di rigenerazione e ricircolo del dialisato noto come sistema REDY, che è stato introdotto per la prima volta nel 1973. Il Ciclosilicato di Zirconio di Sodio è usato per via orale nel trattamento dell’iperkaliemia. È un assorbente selettivo progettato per intrappolare gli ioni di potassio rispetto ad altri ioni in tutto il tratto gastrointestinale.
Una miscela di complessi monomerici e polimerici Zr4+ e Al3+ con Idrossido, Cloruro e Glicina, in sigla AZG, viene utilizzata come preparato antitraspirante in molti prodotti deodoranti. È selezionato per la sua capacità di ostruire i pori della pelle e bloccare la sudorazione.
L’isotopo radioattivo 89Zr è stato sperimentato per il monitoraggio e quantificazione di anticorpi molecolari nella tomografia a emissione di positroni (PET) (un metodo chiamato “immuno-PET”). L’immuno-PET ha attualmente raggiunto un avanzato sviluppo tecnico e sta entrando nella fase di applicazioni cliniche su larga scala.
Ruolo biologico e pericolosità dello Zirconio
Sebbene il ruolo biologico dello Zirconio non sia noto, il corpo umano contiene, in media, 250 milligrammi di zirconio e l’assunzione giornaliera è di circa 4,15 milligrammi (3,5 milligrammi dal cibo e 0,65 milligrammi dall’acqua), secondo le abitudini alimentari. Lo Zirconio è ampiamente distribuito in natura e si trova in tutti i sistemi biologici, ad esempio: 2,86 μg/g nel grano integrale, 3,09 μg/g nel riso integrale, 0,55 μg/g negli spinaci, 1,23 μg/g nelle uova e 0,86 μg/g nella carne macinata di manzo.
Inoltre, lo Zirconio è comunemente usato anche nella purificazione dell’acqua (ad es. controllo dell’inquinamento da fosforo, acqua contaminata da batteri).
Contattaci per saperne di più
C.I.R.T.A.A. srl è lieta di approfondire l’argomento e rispondere alle tue domande.